アジド基の特性を利用した光親和性標識法の開発
生物活性を持つ新しい小分子を見つけたとき、それがどんなタンパク質を標的としているのか?創薬研究などにおいて、最初にぶつかる重要かつ難しい問題です。
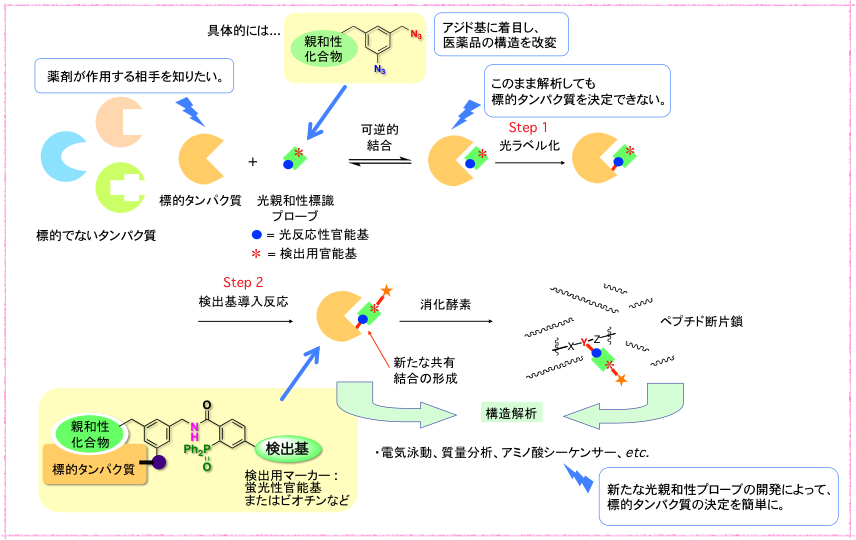
薬剤が作用している相手を知るためには、多数の標的でないタンパク質の中から、標的タンパク質のみを捕捉しなければなりません。しかし、標的タンパク質と薬剤との相互作用は可逆的な弱い結合であるために、そのままでは標的タンパク質を決定することはできません。そこで、他のタンパク質とは反応せずに標的のタンパク質だけ反応する仕掛けが必要です。これに対して、光親和性標識プローブを用いると、 標的タンパク質とプローブとが複合体を形成しているところに光照射を行うことで、近傍にある標的タンパク質内と共有結合を形成します。
当研究グループでは、アジド基(-N3)の性質を巧みに利用した光親和性標識法であるジアジドプローブ法を開発し(Org. Biomol. Chem. 2004, 2, 637.)、本手法を用いていくつかの薬剤の標的タンパク質を決定してきました。最近では、他の研究グループも本手法を利用してくれるようになってきました(K. A. Stubbs, et al., Chem. Commun. 2011, 47, 5037.)。本手法の特徴は、用いるプローブが「光反応による標的タンパク質との共有結合形成(捕獲)」と「標的タンパク質への検出基の導入(標識)」という2度の異なる反応を行える2種類のアジド基を有することです。(詳しくはこちらをご覧ください)

具体的には、生物活性化合物の構造の一部分を改変し、2種類のアジド基を導入した分子プローブを用いて、標的タンパク質を捕獲します。
(1)標的タンパク質を含む細胞抽出液などに分子プローブを作用させ、これに紫外光を照射すると、光反応によって芳香族アジド部位で共有結合が形成され、「標的タンパク質+分子プローブ」となった新しい化合物が生じます。(標的タンパク質と生物活性化合物との相互作用は一般に可逆であるため、共有結合の形成なしでは、ほとんどの場合、精製過程で標的タンパク質と生物活性化合物とが分離してしまいます。)このとき、脂肪族アジド基は光反応せず、生成物中に残っている点が重要です。
(2)次に、残った脂肪族アジドを目がけた反応によって、無数のタンパク質の中から、「標的タンパク質+分子プローブ」を見つけ出します。例えば、Staudinger ligationと呼ばれるリン化合物との反応によって、蛍光性化合物などと連結することができます。こうすることで、目的のタンパク質だけに蛍光部位が導入されるため、それが目印となり、標的タンパク質のみを精製し、その構造を決めることができます。
実際に本手法を利用することで、以下のようなプローブを用いて薬剤の標的タンパク質を決定することができました。

わざわざ2度の標識を行う利点は、「小は大を兼ねる」という発想に基づいています。タンパク質による小分子の認識は大雑把でもあり、繊細でもあります。オリジナルの生物活性化合物と全く同じ分子でなくても認識してくれますが、認識に必要な部位が欠けていたり、タンパク質が小分子を認識する「ポケット」の大きさに収まらなくなると、認識されなくなってしまい、目的としている生物活性が失われてしまいます。そのため、最初から蛍光団などの検出基を導入した分子プローブでは、標的タンパク質に認識されないことが多いわけです。従って、ある生物活性を発見し、そのオリジナル化合物をもとに標的タンパク質捕獲用の分子プローブをつくる段階になって、新たに導入した光反応性官能基や検出用官能基が邪魔をして、生物活性が大きく低下してしまう場合が多く見られます。
こういった理由から、最小限の構造改変で、極性にも余り変化を与えることなく、分子プローブを設計する必要があります。そこで、「小は大を兼ねる」です。小さな官能基であるほど、オリジナルの生物活性が維持しやすく、最適な分子プローブが創出できると考え、我々は2つのアジド基を有するベンゼン環(ジアジドユニット)の利用を考案しました。多くの生物活性化合物中に含まれるベンゼン環に着目し、その化合物の認識を邪魔しない位置に2種類のアジド基(アジド基とアジドメチル基)を導入すれば、標的タンパク質が決められる分子プローブに早変わり、という単純なものです。アジド基は窒素原子が3つ直線に並んだ小さな官能基で、極性をほとんど持たず、生体内には存在しない(bioorthogonalな)官能基であるため、分子プローブ化に利用するのに最適です。単純な発想ではありますが、とくに低分子薬剤など、大きな検出基が利用できない系において力を発揮する優れた手法と自負しています。
もちろん、アジド化合物は爆発性を有するものが多く、取扱いには注意を要しますが、本手法でも利用しているように、大変、魅力的な反応性をもっております。(当研究室でも、防爆板の利用・大量合成の回避など、細心の注意を払っています。爆発してしまったことは未だありませんが油断大敵。)今後、安全性も鑑みたアジド基の導入法やジアジド部位を有する新しいビルディングブロックの開発などを行うことで、本手法をより魅力的な方法論にしていきたいと考えています。



